COVID-19 예방접종 후 자가면역 수포성 피부병: 5가지 사례 시리즈
게시 날짜: 2022년 3월 13일 (기록 보기)
DOI: 10.7759/curus.23127
이 기사를 다음과 같이 인용하십시오: Hali F, Araqi L, Marnissi F, et al. (2022년 3월 13일) COVID-19 예방접종 후 자가면역 수포성 피부병: 5가지 사례 시리즈. 큐레우스 14(3): e23127. doi:10.7759/cureus.23127
요약
자가면역 수포성 질환(AIBD)은 피부 및 점막 소포, 수포 및 미란을 특징으로 하는 이질적인 질병 그룹입니다. 백신을 포함한 여러 요인이 이 질병을 유발할 수 있습니다. 그러나 이 개체는 매우 드물다. 우리는 코로나바이러스 질병 2019(COVID-19)에 대한 예방접종이 유전적으로 소인이 있는 개인에서 면역학적 반응을 유발할 수 있다고 가정했습니다. 우리는 COVID-19 백신에 의해 유발된 새로운 발병 자가면역 수포성 질병의 5건의 사례를 보고합니다. 임상 및 조직병리학적 검사에서 3명의 환자에서 수포성 천포창(BP)의 진단이 확인되었고 다른 2명의 환자에서 천포창이 확인되었습니다. 프랑스 전가법에 따르면 약물감시 조사 결과 백신에 대한 I5B4 인과관계 평가 점수가 나타났으며 모든 환자에 대해 가능성이 높은 것으로 해석되었습니다. 백신으로 유발된 자가면역 수포성 피부병의 진단이 매우 의심스러웠습니다. 한 환자의 상태는 더모코르티코이드 단독으로 개선된 반면, 다른 4명은 0.5mg/kg/일의 경구 코르티코스테로이드 요법이 필요하여 양호한 결과를 얻었습니다.
소개
자가면역 수포성 질환(AIBD)은 종종 피부 및 점막 소포, 수포 및 미란으로 나타나는 이질적인 질병 그룹입니다. 상태 뒤에 있는 병원성 메커니즘은 desmosomes 및 hemidesmosomes를 표적으로 하는 자가항체의 존재를 포함합니다. 이러한 구조 단백질은 표적이 되며 천포창에서 표피 내이어서 물집이 표면적이고 부서지기 쉬운 반면 수포성 천포창(BP)에서는 표피 아래에 있어 긴장된 수포가 형성됩니다. 백신을 포함하여 AIBD를 유발하는 몇 가지 요인이 알려져 있습니다 [1]. 세계보건기구(WHO)는 2020년 3월 코로나바이러스 감염증 2019(COVID-19)를 세계적 대유행으로 선언했으며 전 세계적으로 수백만 명의 사람들이 이 질병의 영향을 받았습니다. 2021년 1월 모로코에서 백신 접종 캠페인이 시작되어 자가면역 질환이 눈에 띄게 증가했습니다 [2] . 이 보고서에서 우리는 COVID-19 백신에 의해 촉발된 새로운 발병 AIBD 사례 5건에 대해 논의합니다. 이 중 3건은 BP가 있고 다른 2건은 천포창이 있습니다. 5건 모두 약물감시 조사를 통해 진단이 확정되었습니다.
---------------------------------------------------------------
미란미란의 정의, 증상, 원인 및 치료에 관한 사항은 다음과 같습니다.
정의 : 미란(erosion)이란 출혈은 되지 않고 광범위하고 얇게 표피의 표면이 벗겨진 상태를 말한다.
증상 : 표피가 전신에 걸쳐서 광범위하고 얇게 벗겨진다.
원인 : 염증성 유방암, 무좀균, 당뇨병 및 순환불량에 관련되어 발병한다.
치료 : 병변을 냉각시키고 건조시키므로 염증을 완화하고 소양감을 감소시키고 청정작용을 하는 습포 방법과 예방하는 차원인 땀띠분제를 사용한다.
--------------------------------------------------------------------------------------------------------------------------------
사례 발표
사례 1
51세 남성이 Oxford AstraZeneca COVID-19 백신의 첫 번째 부스터를 투여한 지 7일 후에 나타난 광범위한 수포성 발진의 관리로 입원했습니다. 특별한 병력은 없었고 다른 약물을 복용하고 있지 않았습니다. 임상 검사에서 몸통, 등 및 다리의 두드러기 플라크와 관련된 미만성 긴장 수포의 존재가 나타났습니다. 수포 후 미란과 피부 표면의 70%에 영향을 미치는 코카드 같은 병변이 관찰되었습니다. Nikolsky 기호는 양수였습니다(그림 1 ). 환자는 또한 협측 점막에 여러 번의 미란이 있었습니다(그림 2 ).
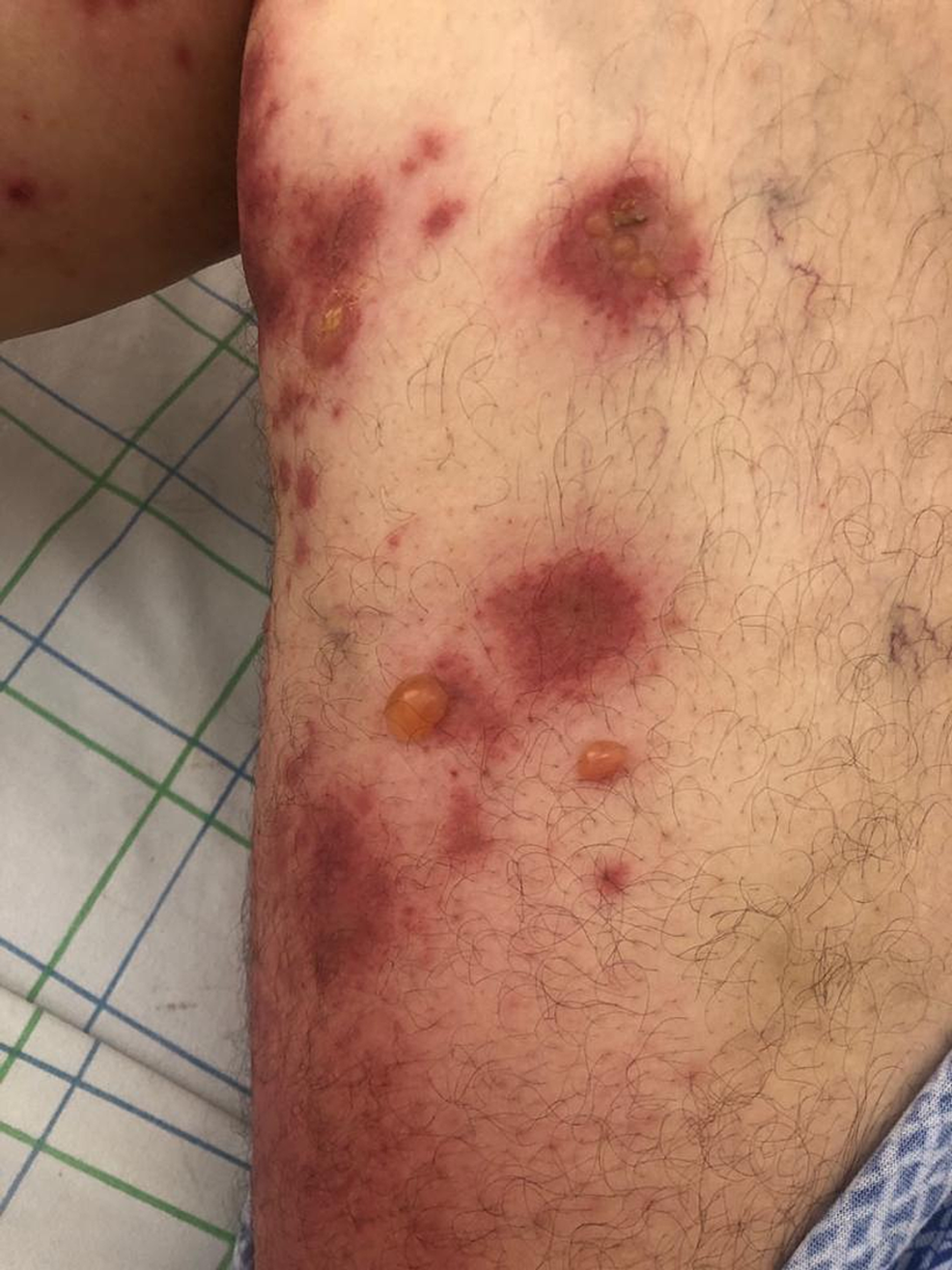
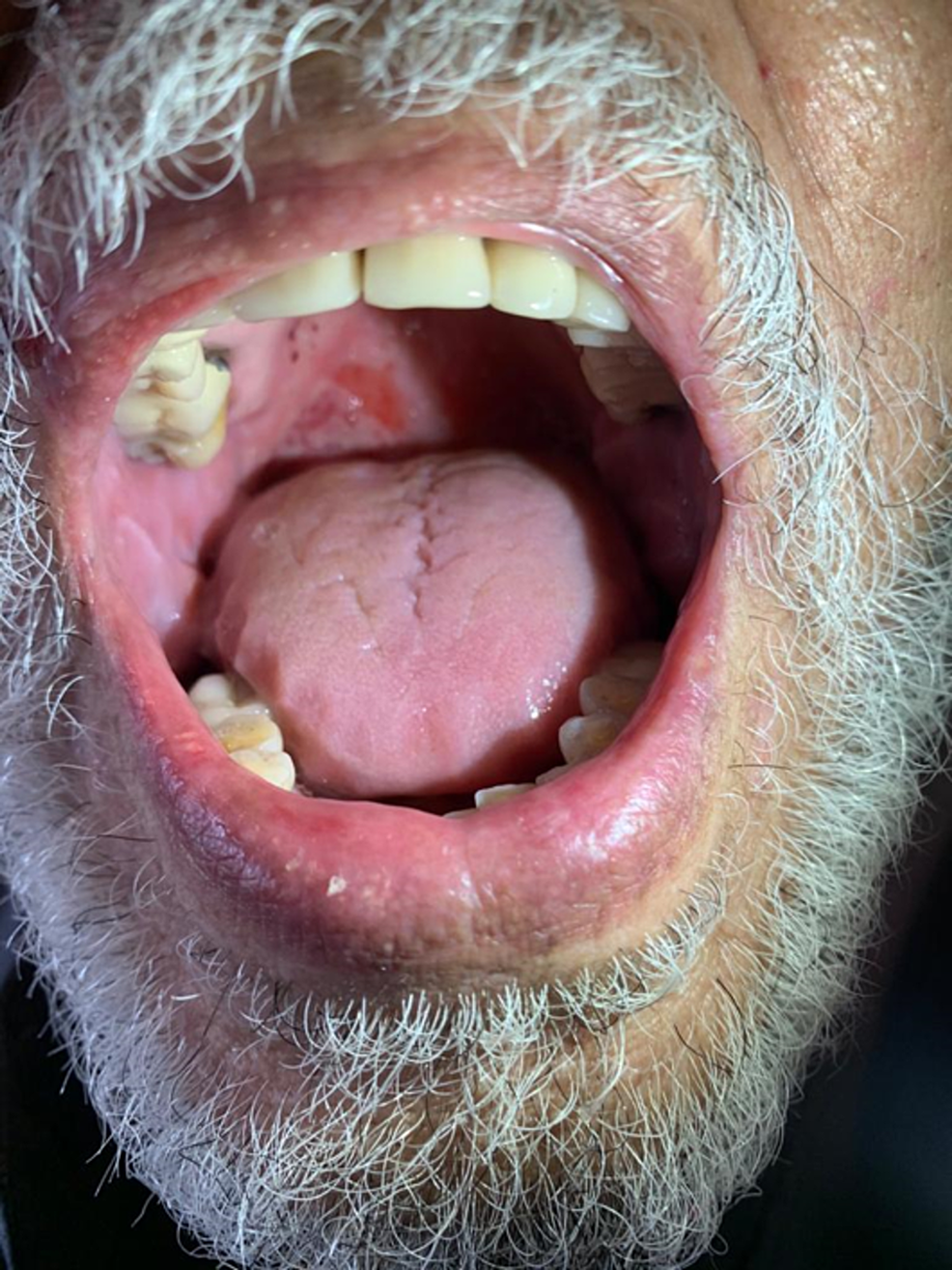
조직학적 검사는 표피하의 표피가 혈관주위 염증 침윤물과 우세한 호산구를 가진 분열을 보여주었다. 직접 면역형광은 기저막 영역에서 선형 C3 패턴을 갖는 조직 결합 자가항체를 검출했습니다. 환자의 혈청을 사용하여 염분할 정상 인간 피부 기질에 대해 수행한 간접 면역형광 검사에서 BP와 일치하는 순환 면역글로불린 G(IgG)(BP180 항체)가 검출되었습니다. 나머지 실험실 분석에서는 높은 호산구 수치를 제외하고는 정상적인 결과를 보였습니다. 약물감시 부서에 통보하고 즉시 철저한 조사에 착수하여 프랑스 전가법에 따라 백신에 대한 I5B4 인과관계 평가 점수를 나타냈다 [3]. 백신으로 유발된 혈압의 진단은 매우 의심스러웠다. 환자는 6주 동안 매일 프레드니손 30mg(매일 0.5mg/kg)을 투여한 후 매주 5mg씩 감량한 후 완전히 중단했습니다. 수포의 완전한 해결은 치료 4주 후에 이루어졌습니다.
사례 2
54세 여자가 접종 부위에 광범위한 홍반성 발진과 수포가 발생한 1주일의 병력을 내원하였다. 그녀는 발진이 시작되기 3일 전에 왼쪽 팔뚝에 코로나19 백신(옥스포드 아스트라제네카)의 첫 번째 접종을 맞았습니다. 그녀는 이전에 특별한 병력이 없었습니다. 발진은 작은 국소 수포와 함께 주사 부위에서 시작되었습니다. 그런 다음 왼쪽 팔뚝에서 복부, 등, 다리 아래로 퍼졌습니다. 입원 시 신체 검사에서 양팔, 복부 및 허벅지에 두드러기 플라크와 관련된 긴장된 수포가 나타났고 Nikolsky 징후가 양성이었습니다(그림 3 ).
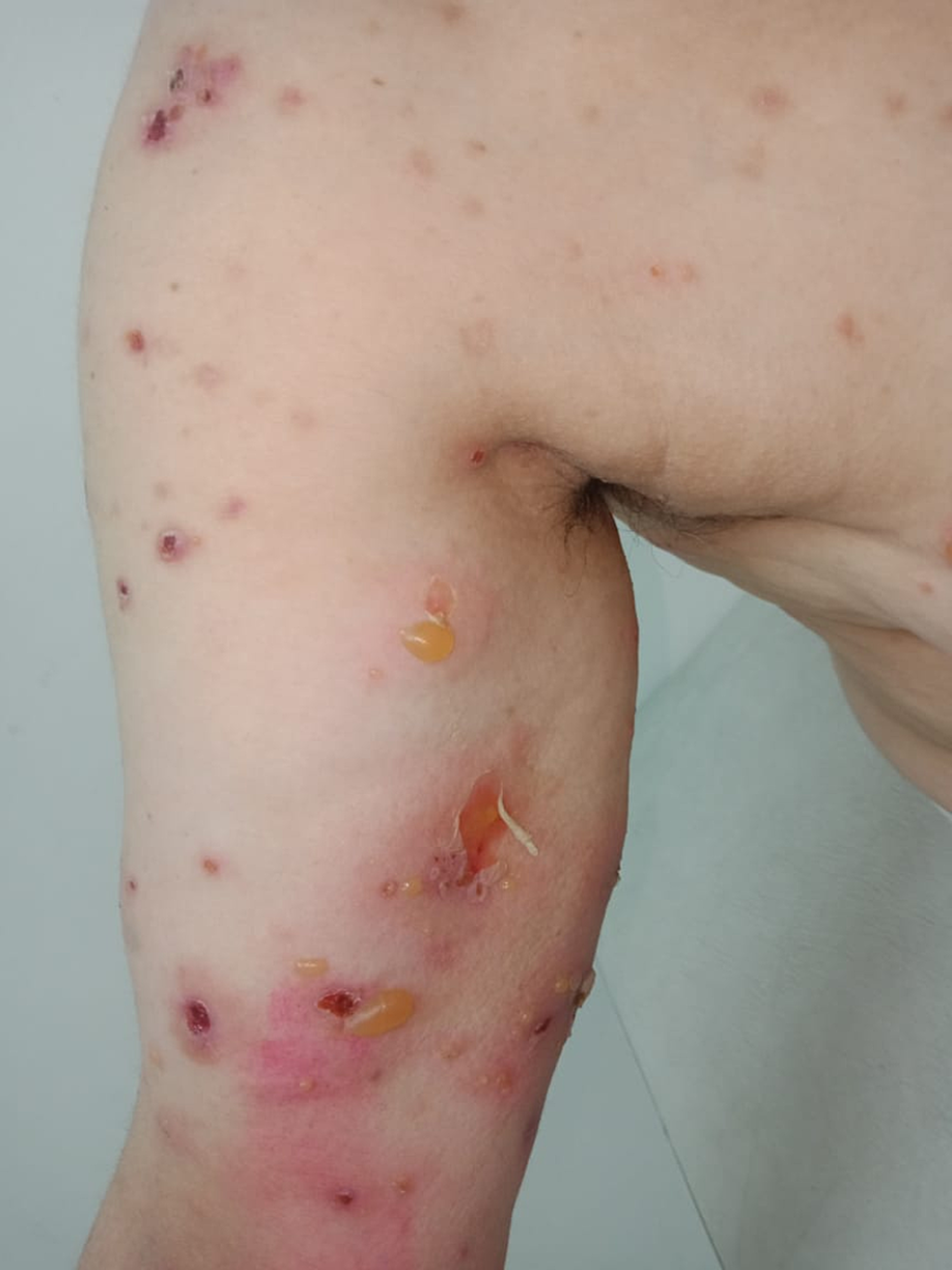
그녀는 또한 입천장에 미란이 있었습니다. 조직학적 검사는 표피하의 표피가 혈관주위 염증 침윤물과 우세한 호산구를 가진 분열을 보여주었다. 직접 및 간접 면역형광 모두 선형 IgG 및 C3에서 양성이었고 BP와 일치했습니다. 생물학적 검사는 2200/mm 3 의 호산구 수치를 나타냈습니다 . 이전에 인용된 약물감시 프로토콜 [3] 에 따르면, 인과관계 점수 평가는 백신에 대해 I5B4였으며, 이는 백신 유발성 혈압의 진단을 매우 시사한다. 환자는 호전된 국소 코르티코스테로이드(clobetasol propionate 0.05%)를 투여받았습니다. 백신 부스터는 금기가 아니었지만 환자가 거부했습니다.
사례 3
환자는 68세 남자로 20년 동안 고콜레스테롤혈증의 병력이 있었고 다른 특별한 개인 또는 가족력은 없었다. Oxford AstraZeneca COVID-19 백신의 첫 번째 접종을 받은 지 2주 후, 그는 접종 부위에 물집이 생겼고, 처음에는 외상 후 병변으로 오진되었습니다. 첫 번째 접종 후 3주 이내에 접종한 부스터 백신을 접종한 지 7일 만에 팔다리와 몸통에 새로운 물집이 생겨 증상이 악화되었습니다. 신체 검사에서 몸통과 팔다리의 직경 3-10cm를 측정하는 홍반성 기저부에서 긴장된 수포와 수포 후 미란이 발견되었으며 Nikolsky 징후가 양성이었습니다(그림 4 ).
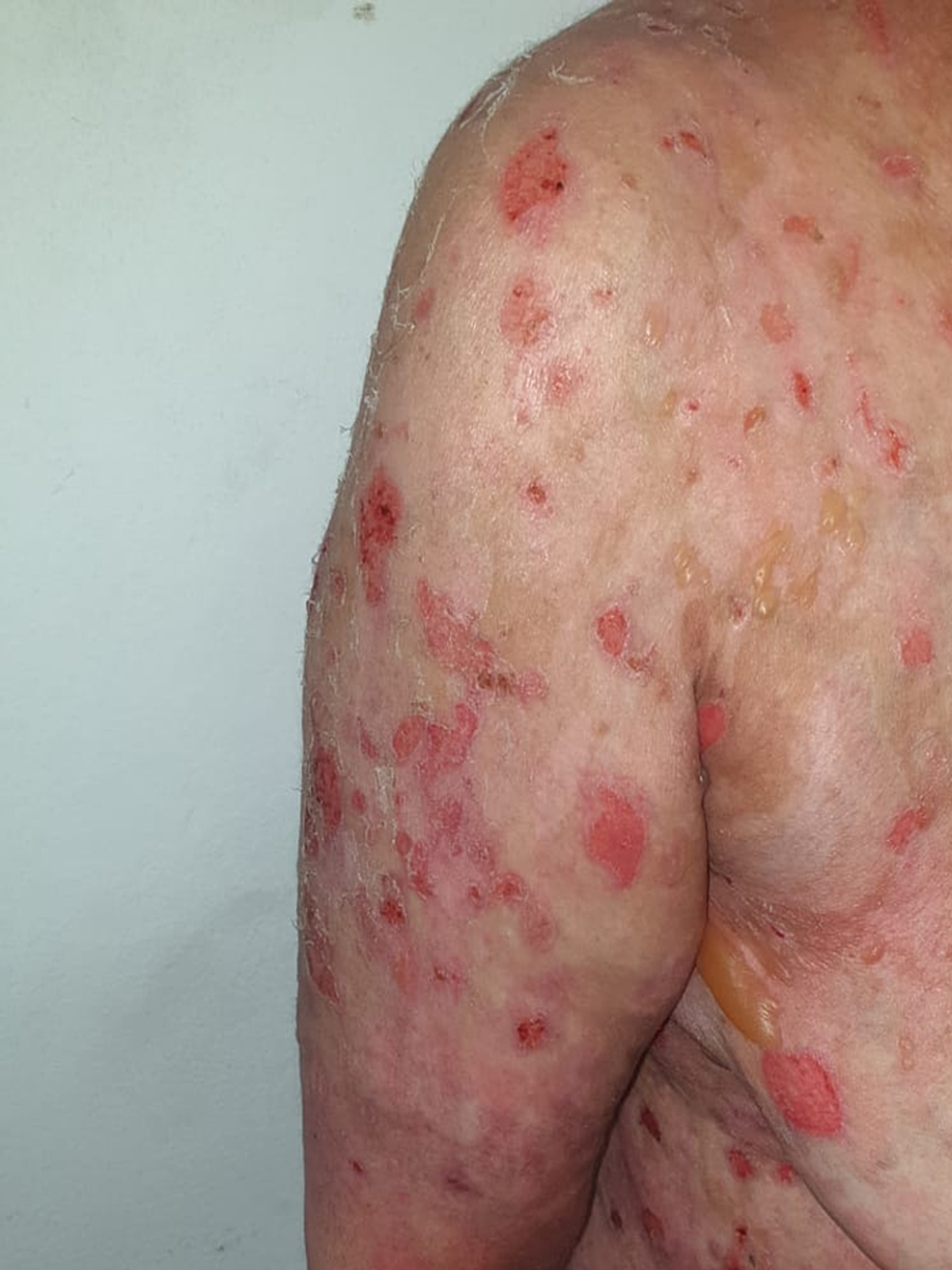
구강 및 생식기 점막의 미란도 관찰되었습니다. 나머지 임상검사는 정상이었다. 혈액 검사가 수행되었으며, 2750/mm 3 에서 높은 호산구 증가증을 제외하고는 정상으로 돌아왔습니다 . 조직학적 검사에서 호산구의 염증성 침윤이 있는 표피하 수포가 나타났습니다. 직접 면역형광법은 기저막을 따라 선형 C3 패턴을 나타냈다. BP 진단이 내려졌다. 전가율 점수는 I5B4로 백신에 의해 유발된 혈압을 시사합니다. 환자는 한 달 동안 30mg/일(0.5mg/kg/일)의 경구 코르티코스테로이드 요법을 필요로 했으며, 이는 유리한 결과를 가져왔습니다. 그 후 점진적인 퇴행이 시작되었습니다.
사례 4
50세 여성이 화이자/바이오엔텍 코로나19 백신 접종 15일 만에 나타난 전신미란으로 내원했다. 그녀는 특별한 병력이 없었습니다. 임상 검사에서 특히 몸통, 등 및 두피(피부 영역의 75%를 덮음)에서 광범위한 수포 후 미란이 나타났으며 양성 Nikolsky 징후가 나타났습니다(그림 5 ).
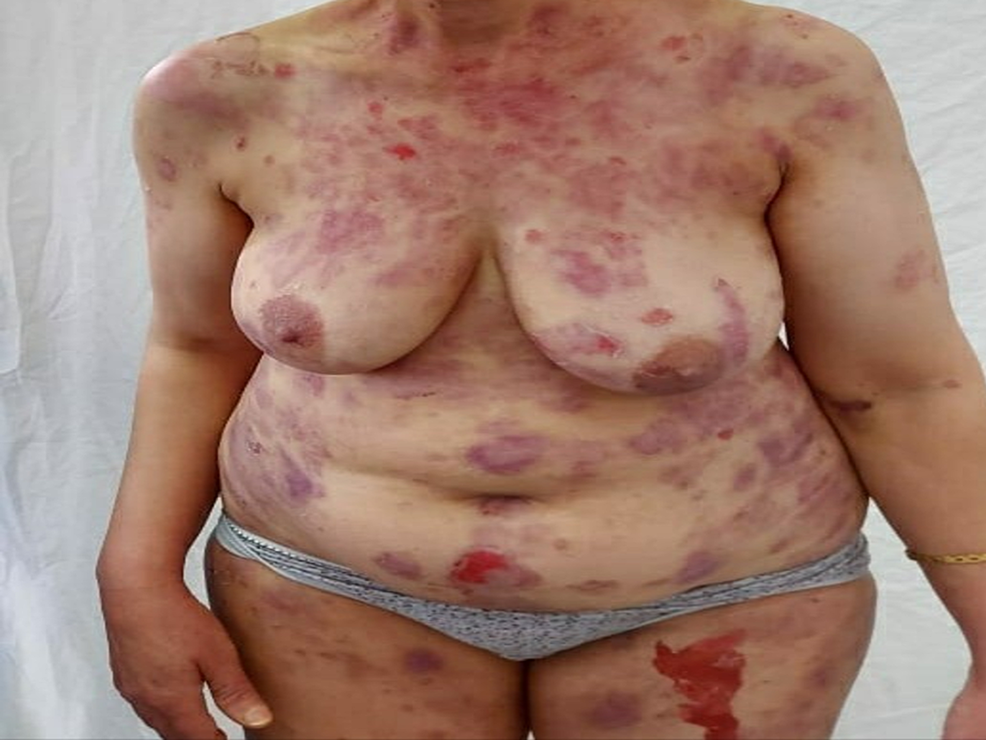
그녀는 점막 침범이 없었습니다. 조직학적 검사는 손상되지 않은 기저층과 표피내 호산구가 있는 표피 수포 과정을 보여주었다. 직접면역형광은 세포내 IgG와 C3를 보였고, 간접면역형광은 항세포간물질항체 양성으로 엽면천포창을 나타냈다. 약물감시 조사에서 백신에 대한 인과관계 점수가 I5B4로 결정되었으며, 이는 백신 유발 천포창의 진단을 시사합니다. 환자는 65mg/day(1mg/kg/day)의 경구 코르티코스테로이드 요법을 받았으며 치료 3주 후에 병변이 완전히 해결되었습니다.
사례 5
10년 동안 우울증을 앓아온 58세 여성이 화이자/바이오엔텍의 코로나19 백신 1차 접종 1개월 후 전신에 미란이 생겨 입원을 요하는 내원했다. 신체 검사에서 그녀의 얼굴, 몸통, 복부, 등, 엉덩이 및 양쪽 다리에 광범위한 미란성 병변이 나타났습니다(그림 6 ).
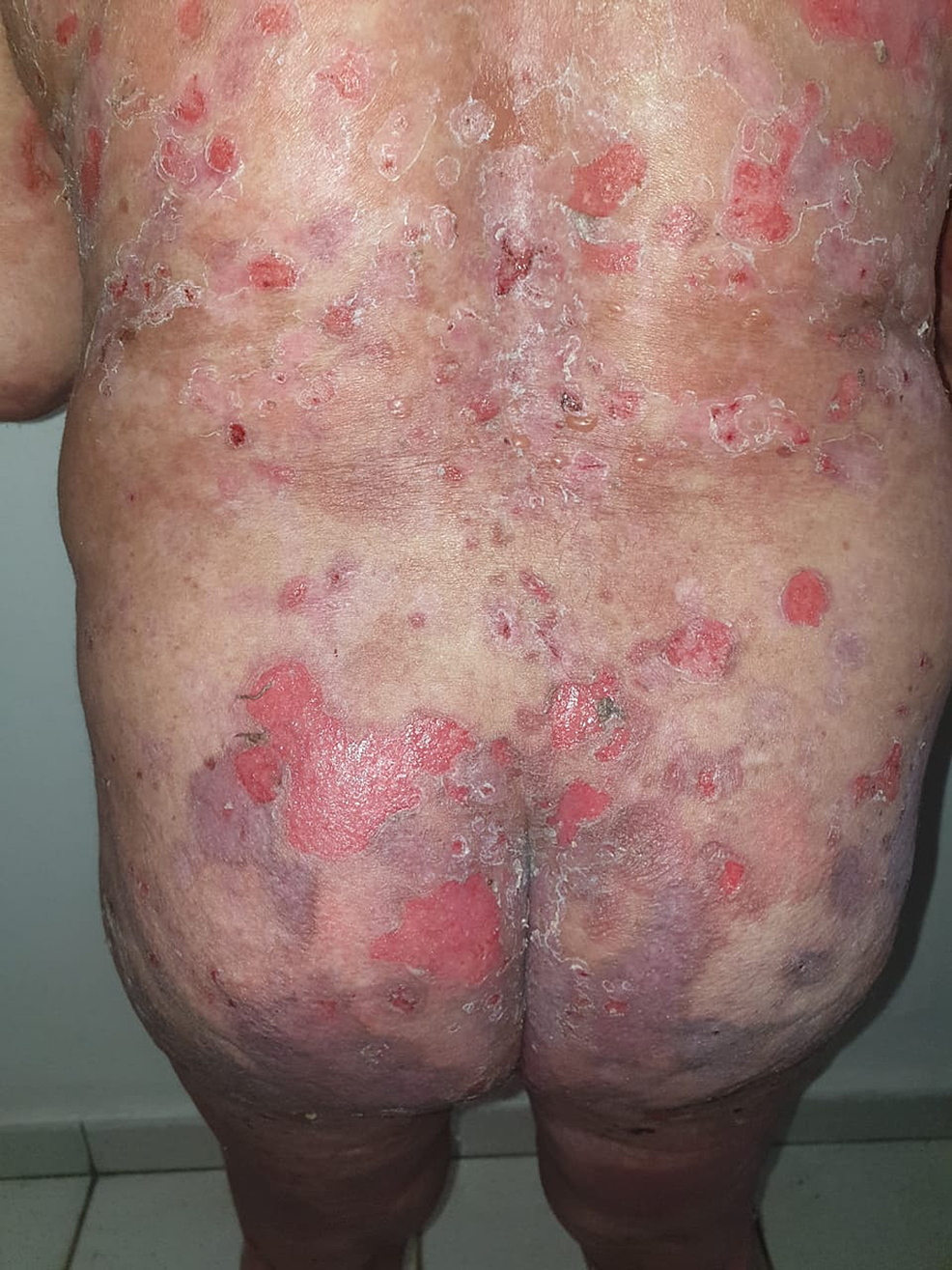
그녀는 또한 구강 및 생식기 점막에 미란이 있었습니다. 복부 병변의 조직학적 검사에서 가피세포 용해가 있는 표피내 소포와 미만성 혈관주위 진피 림프구 및 호산구성 침윤이 나타났습니다. 직접 면역형광은 표피 세포 표면 막에 IgG 및 C3의 침착을 입증했습니다. 이러한 소견을 바탕으로 심상성 천포창의 진단이 내려졌습니다. 백신과 sertraline 모두의 전가 가능성이 연구되었고 조사 결과 백신이 관련되었습니다. 환자의 상태는 55mg/일(1mg/kg/일)의 코르티코스테로이드 요법으로 개선되었습니다. 그녀는 여전히 부스터 주사를 맞을 예정입니다.
표 1 은 COVID-19 백신 접종 후 새로 발병한 AIBD 환자의 데이터를 요약한 것입니다.
| 환자 | 나이/성별 | 관련 백신 | 발병 시간 | AIBD | 점막 침범 | 영향을 받는 피부 표면 | 호산구 수 | 치료 |
| 환자 1 | 51/남 | Oxford AstraZeneca COVID-19 백신 2차 접종 | 7 일 | 수포성 류천포창 | 예 | 70% | 3900 / mm3 | 코르티코스테로이드 요법 0.5 mg/kg/일 |
| 환자 2 | 54/F | Oxford AstraZeneca COVID-19 백신의 첫 번째 접종 | 3 일 | 수포성 류천포창 | 예 | 30% | 2200/ mm3 | 더모코르티코이드 |
| 환자 3 | 68/남 | Oxford AstraZeneca COVID-19 백신 2차 접종 | 7 일 | 수포성 류천포창 | 예 | 50% | 2750 / mm3 | 코르티코스테로이드 요법 0.5 mg/kg/일 |
| 환자 4 | 50/F | 화이자/바이오엔텍 코로나19 백신 2차 접종 | 15 일 | 폴리아세우스 천포창 | 아니 | 75% | 500/ mm3 | 코르티코스테로이드 요법 1 mg/kg/일 |
| 환자 5 | 58/F | 화이자/바이오엔텍 코로나19 백신 1차 접종 | 1 개월 | 천포창 | 예 | 80% | 850 / mm3 | 코르티코스테로이드 요법 1 mg/kg/일 |
COVID-19: 코로나바이러스 질병 2019; AIBD: 자가면역 수포성 질환
논의
AIBD의 발병은 주로 면역계의 과자극 상태를 생성함으로써 다양한 요인에 의해 생성될 수 있습니다 [1] . 백신은 면역 체계에 영향을 미치는 환경 요인의 실질적인 구성 요소를 형성합니다. 면역 체계의 과도하게 자극된 상태와 유전적으로 소인이 있는 상태의 조합은 AIBD를 유발할 수 있습니다. 중증급성호흡기증후군 코로나바이러스 2(SARS-CoV-2) 바이러스 막의 면역원성 단백질과 인간 세포외 분자 간의 유사성으로 인한 교차 반응성은 그럴듯한 유발 요인일 수 있습니다 [4] .
BP는 홍반성 기저부에 긴장성 수포가 나타나고 hemidesmosomes의 BP180 및 BP230 항원에 대한 순환 IgG의 존재가 특징입니다 [5] . 그러나 BP 발병에서 백신의 역할은 완전히 밝혀지지 않았습니다. 백신, 특히 불활성화 백신(예: Oxford AstraZeneca COVID-19 백신)이 면역을 제공하는 주요 메커니즘은 B-림프구를 자극하여 구조 단백질에 대한 항체를 생성하는 체액 경로를 포함합니다 . 6] . 더욱이 백신 접종으로 인한 염증은 기저막의 파괴로 이어져 항-지하막 특이적 항체가 생성될 수 있다 [7].. 성인과 어린이에 대한 문헌에서 백신 접종 후 BP의 소수 사례만 보고되었습니다 [8] . 우리의 관찰과 문헌 [9] 에 대한 검토에 따르면 , 유도된 혈압은 큰 수포, 양성 Nikolsky 징후, 점막 침범 및 높은 호산구 수를 특징으로 하며, 이는 모두 우리 환자에서 발견되었습니다.
천포창의 경우 순환하는 자가항체가 데스모솜 조립에 관여하는 막관통 단백질(desmogleins)에 결합하여 가극세포 용해를 유발합니다 [10] . 분자 모방의 메커니즘 외에도 mRNA 백신(예: 천포창 환자에게 투여된 Pfizer/BioNTech COVID-19 백신)은 일련의 면역학적 사건을 일으켜 궁극적으로 비정상적 활성화로 이어질 수 있습니다. 선천성 및 후천성 면역계 [11] . 이것은 항바이러스 반응을 매개하는 X-연관 유전자의 과발현과 면역계에 대한 에스트로겐의 자극 효과로 인해 젊은 여성에게 특히 해당될 수 있습니다. 천포창 환자는 모두 여성이었습니다 [12] .
Kasperkiewicz et al. SARS-CoV-2에 대한 백신과 자가면역의 진화 사이의 연관성을 조사했습니다. 혈청 샘플에서 주요 면역수포성 자가항원(desmoglein 1, desmoglein 3, envoplakin, BP180, BP230 및 type VII 콜라겐)에 대한 자가항체를 테스트했습니다. Pfizer-BioNTech mRNA COVID-19 백신을 2회 접종한 COVID-19 개인 및 12명의 건강한 혈청 양성 지원자. 결과는 SARS-CoV-2 감염/백신과 AIBD 간의 관계에 대해 논쟁이 있었지만 질병 유발 항체 교차 반응성 이론이 강력하게 제안되었습니다 [13] .
결론
이러한 백신 유도 발현은 아마도 자가항원과 백신이 주입된 항원 사이의 교차 반응성 또는 단순히 보조제의 효과에 기인할 수 있습니다. 우리는 COVID-19에 대한 백신 접종이 유전적 소인이 있는 개인에서 면역학적 반응을 유발한다고 가정합니다. 이러한 유형의 조절 장애는 다른 자가면역 기전에 의해 강화됩니다. COVID-19 백신은 아마도 AIBD의 백신 유발자 목록에 추가되어야 할 필요가 있을 것입니다.
그러나 SARS-CoV-2 감염의 합병증, 예방 접종과 부작용 사이의 인과 관계의 불확실성, 이러한 사건의 희소성을 고려할 때 임상의는 여전히 COVID-19에 대한 완전한 예방 접종을 권장해야 합니다. 1차 및 2차 투여 후 수포 유발. 우리가 관찰한 매우 흥미로운 측면은 새로 발병한 BP 환자에게 비활성화된 COVID-19 백신이 투여된 반면 유도 천포창 환자는 mRNA COVID-19 백신 접종 후에 진단되었다는 것입니다. 최근 mRNA 코로나19 백신 접종 후 BP 발생 사례가 보고된 점을 감안하면 이는 단순한 우연의 일치일 수 있다.
참고문헌
- Segal Y, Shoenfeld Y: 백신 유발 자가면역: 분자 모방 및 면역 교차 반응의 역할 . Cell Mol Immunol. 2018, 15:586-94. 10.1038/cmi.2017.151
- Sachinidis A, Garyfallos A: COVID-19 백신 접종은 때때로 자가면역 현상을 유발할 수 있으며 아마도 연령 관련 B 세포를 유도할 수 있습니다 . Int J Rheum Dis. 2022, 25:83-5. 10.1111/1756-185X.14238
- Moore N, Berdaai D, Blin P, Droz C: 약물 감시 - 다음 장 . 요법. 2019, 74:557-67. 10.1016/j.therap.2019.09.004
- Drenovska K, Vassileva S, Tanev I, Joly P: 자가 면역 수포 질환에 대한 COVID-19의 영향 . 클린 더마톨. 2021, 39:359-68. 10.1016/j.clindermatol.2021.01.007
- Pérez-López I, Moyano-Bueno D, Ruiz-Villaverde R: 수포성 천포창 및 COVID-19 백신 . 메드 클린(바크). 2021, 157:e333-4. 10.1016/j.medcli.2021.05.005
- Moro F, Fania L, Sinagra JL, Salemme A, Di Zenzo G: 수포성 천포창: 방아쇠 및 소인 . 생체 분자. 2020, 10:1432. 10.3390/biom10101432
- Jindal A, Nayak SU, Shenoi SD, Rao R, Monappa V: 광견병 백신에 의해 유발된 수포성 천포창 . 인디언 J 더마톨 베네레올 레프롤. 2020, 86:66-8. 10.4103/ijdvl.IJDVL_666_18
- Bisherwal K, Pandhi D, Singal A, Sharma S: 예방 접종 후 유아 수포성 천포창 . 인도 소아과. 2016, 53:425-6. 10.1007/s13312-016-0867-3
- Stavropoulos PG, Soura E, Antoniou C: 약물 유발 천포창: 문헌 검토 . J Eur Acad Dermatol Venereol. 2014, 28:1133-40. 10.1111/jdv.12366
- Gniadecki R: 천포창의 발병기전에서 Desmoglein 자가면역 . 자가면역. 2006, 39:541-7. 10.1080/08916930600971505
- Damiani G, Pacifico A, Pelloni F, Iorizzo M: COVID-19 백신의 첫 번째 접종은 천포창과 수포성 천포창 발적을 유발할 수 있습니다. 따라서 두 번째 접종은 금기입니까? . J Eur Acad Dermatol Venereol. 2021, 35:e645-7. 10.1111/jdv.17472
- Goriely S, Goldman M: 내성에서 자가면역으로: 조기 예방 접종에 위험이 있습니까? . J Comp Pathol. 2007, 137:S57-61. 10.1016/j.jcpa.2007.04.013
- Kasperkiewicz M, Bednarek M, Tukaj S: 사례 보고: 순환하는 항-SARS-CoV-2 항체는 천포창 또는 천포창 자가항원과 교차 반응하지 않습니다 . 프론트 메드(로잔). 2021, 8:807711. 10.3389/fmed.2021.807711
'취미 > 건강' 카테고리의 다른 글
| 유기농 염색약이 더 안전한가요? (0) | 2022.09.17 |
|---|---|
| 대부분의 사람들이 오메가 지방산에 대해 모르는 것 (0) | 2022.09.17 |
| 인간 혈액에서 마스크의 미세 플라스틱 관찰 (0) | 2022.03.27 |
| [뉴스] 코로나 백신, 간세포에 들어가 (0) | 2022.03.08 |
| 자연면역자와 접종자 차이 (0) | 2022.02.16 |